熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Tissue oxygen partial pressure as a viability metric for ex vivo brain tissue slices
組織氧分壓作為離體腦組織切片的活力指標(biāo)
來(lái)源:Journal of Neuroscience Methods 396 (2023) 109932
摘要內(nèi)容
本研究提出了一種基于組織氧消耗率的離體腦切片存活度評(píng)估新方法。通過(guò)測(cè)量小鼠皮層腦切片中的最低氧分壓(pO????),結(jié)合氧消耗率計(jì)算和2,3,5-三苯基氯化四氮唑(TTC)染色驗(yàn)證,發(fā)現(xiàn):
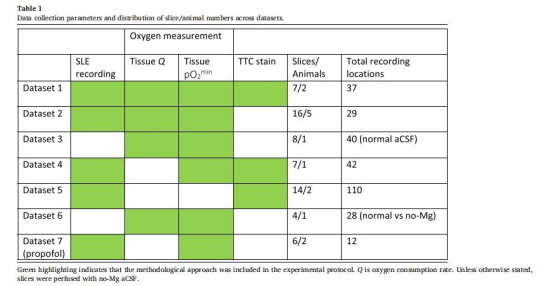
pO????與氧消耗率強(qiáng)相關(guān)(無(wú)鎂人工腦脊液(aCSF)中R2=49.7%,正常aCSF中R2=42.1%),表明pO????可作為氧消耗的簡(jiǎn)易替代指標(biāo)。
pO????與TTC染色一致性高:氧消耗率越高(組織越健康),TTC染色越深(圖4a);pO????越低,TTC染色越深(圖4b)。
癲癇樣事件(SLE)頻率與氧消耗率正相關(guān)(R2=44.8%),而傳統(tǒng)指標(biāo)(如SLE振幅)與存活度無(wú)關(guān)。
研究目的
解決離體腦切片實(shí)驗(yàn)中組織存活度評(píng)估的可靠性問(wèn)題:
驗(yàn)證pO????能否作為簡(jiǎn)單、直接的存活度指標(biāo)。
對(duì)比pO????與傳統(tǒng)電生理指標(biāo)(如SLE振幅)的優(yōu)劣。
探索氧消耗與神經(jīng)活動(dòng)(如SLE)的關(guān)系。
研究思路
模型設(shè)計(jì):
使用400μm厚小鼠皮層腦切片,分為無(wú)鎂aCSF(誘導(dǎo)SLE活動(dòng))和正常aCSF(靜息狀態(tài))兩組。
通過(guò)丹麥Unisense微電極(50μm尖端)測(cè)量切片深度氧分壓。
多維度驗(yàn)證:
氧消耗率(Q):基于Fick擴(kuò)散-消耗模型計(jì)算。
pO????:直接讀取氧分壓剖面最低值。
TTC染色:定性評(píng)估組織活性。
SLE活動(dòng):記錄事件振幅、頻率。
統(tǒng)計(jì)分析:
線性回歸分析pO????與Q、TTC、SLE參數(shù)的關(guān)聯(lián)。
對(duì)比不同條件(如aCSF類型、流速)對(duì)pO????的影響。
測(cè)量數(shù)據(jù)、來(lái)源圖表及研究意義
pO????與氧消耗率相關(guān)性
來(lái)源:圖3a-b(無(wú)鎂/正常aCSF數(shù)據(jù))
pO????是氧消耗率的可靠代理指標(biāo)(無(wú)需復(fù)雜計(jì)算),簡(jiǎn)化存活度評(píng)估流程。
氧參數(shù)與TTC染色的關(guān)聯(lián)
來(lái)源:圖4a-b(TTC vs. Q / pO????)
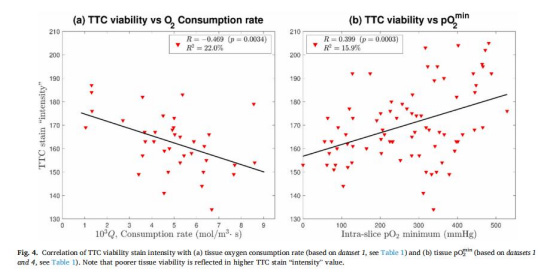
意義:直接證明pO????越低(或Q越高),組織越健康,驗(yàn)證其作為生物學(xué)指標(biāo)的效度。
SLE活動(dòng)與氧消耗的關(guān)系
來(lái)源:無(wú)鎂aCSF數(shù)據(jù)集
意義:SLE頻率(而非振幅)與氧消耗正相關(guān),挑戰(zhàn)傳統(tǒng)電生理指標(biāo)作為存活度標(biāo)準(zhǔn)的可靠性。
流速對(duì)pO????的影響
來(lái)源:流速實(shí)驗(yàn)
意義:低流速(≤2 mL/min)顯著降低pO????,提示實(shí)驗(yàn)需控制aCSF流速≥10 mL/min以減少干擾。
丙泊酚干預(yù)實(shí)驗(yàn)
來(lái)源:數(shù)據(jù)集7(表1)
意義:pO????可預(yù)測(cè)藥物效應(yīng)(如丙泊酚抑制SLE的效果與初始pO????相關(guān)),突顯其在實(shí)驗(yàn)設(shè)計(jì)中的實(shí)用性。
結(jié)論
pO????是理想存活度指標(biāo):
與氧消耗率、TTC染色強(qiáng)相關(guān),且測(cè)量簡(jiǎn)便(無(wú)需全剖面掃描)。
健康組織標(biāo)準(zhǔn):無(wú)鎂aCSF中pO???? ≈0–50 mmHg;正常aCSF中pO???? ≈150–200 mmHg。
傳統(tǒng)電生理指標(biāo)不可靠:
SLE振幅與存活度無(wú)關(guān),頻率雖相關(guān)但模型依賴性高(僅適用于無(wú)鎂aCSF)。
應(yīng)用價(jià)值:
通過(guò)預(yù)實(shí)驗(yàn)測(cè)量pO????,可篩選健康切片或匹配實(shí)驗(yàn)組間存活度,減少結(jié)果偏差(如丙泊酚實(shí)驗(yàn))。
丹麥Unisense微電極測(cè)量數(shù)據(jù)的詳細(xì)解讀
技術(shù)原理與操作
設(shè)備:Clark式氧電極(Unisense,50μm尖端),極化校準(zhǔn)后插入腦片不同深度(圖1e)。
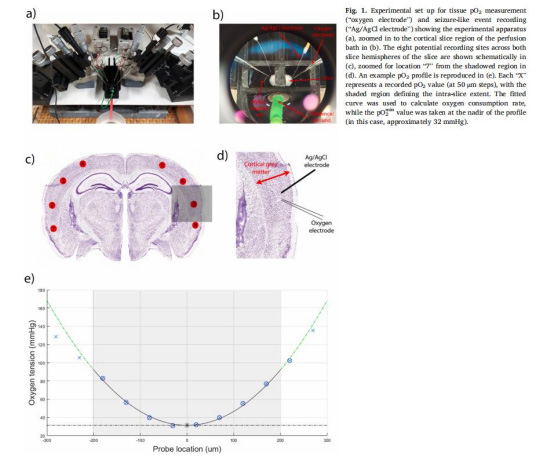
關(guān)鍵步驟:
校準(zhǔn):空氣中(~155 mmHg)和0.1 M抗壞血酸鈉(0 mmHg)兩點(diǎn)校準(zhǔn)。
測(cè)量模式:
全剖面掃描:每50μm步進(jìn),計(jì)算氧消耗率Q(Fick模型)。
pO????快速讀取:定位最低氧分壓位置(通常深度200μm)。
研究意義
量化組織代謝狀態(tài):
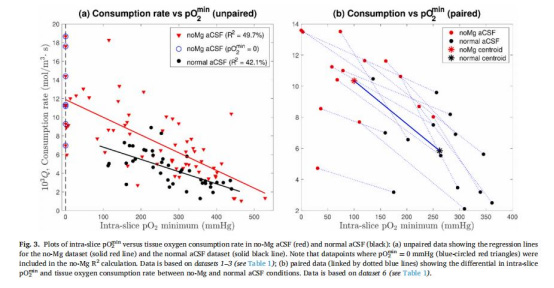
pO????直接反映局部氧需求:健康組織耗氧高→pO????降低(圖3a)。
無(wú)鎂aCSF中pO????比正常aCSF低162 mmHg(圖3b),證明神經(jīng)活動(dòng)顯著增加代謝負(fù)擔(dān)。
解決傳統(tǒng)方法缺陷:
電生理指標(biāo)(如SLE振幅)受同步性等因素干擾,與存活度無(wú)顯著關(guān)聯(lián);pO????提供客觀、定量的生物學(xué)標(biāo)準(zhǔn)。
TTC染色需終止實(shí)驗(yàn),而pO????支持實(shí)時(shí)、無(wú)損監(jiān)測(cè)(圖4a-b)。
優(yōu)化實(shí)驗(yàn)設(shè)計(jì):
揭示aCSF流速對(duì)氧供給的影響(流速≤2 mL/min時(shí)pO????下降22.7 mmHg/mL/min),指導(dǎo)流速設(shè)置(≥10 mL/min)。
提出ΔP = pO????? - pO????作為改進(jìn)指標(biāo)(R2提升至69.5%),消除表面氧分壓波動(dòng)影響(公式4)。

應(yīng)用場(chǎng)景擴(kuò)展:
藥理研究:丙泊酚實(shí)驗(yàn)中,初始pO????預(yù)測(cè)藥物抑制效果(R2=52%),避免存活度混雜因素。
空間異質(zhì)性評(píng)估:多點(diǎn)測(cè)量揭示切片內(nèi)存活度差異(如圖2a位置1 vs. 8),支持精準(zhǔn)區(qū)域選擇。
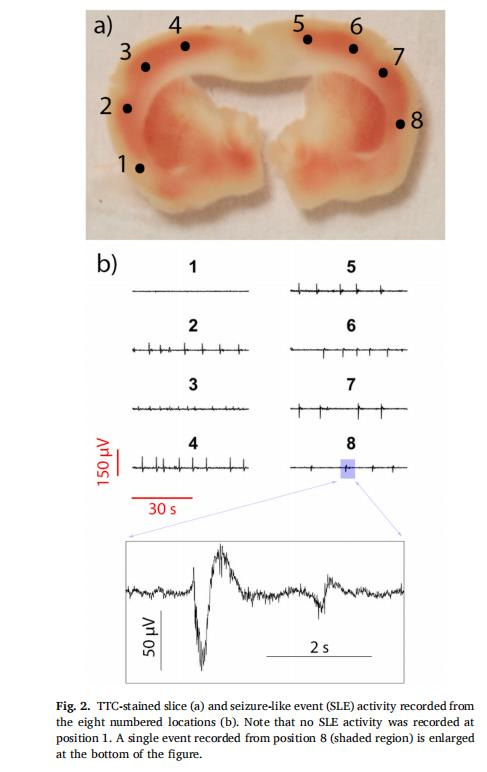
意義:證實(shí)
技術(shù)局限與建議
電極維護(hù):玻璃尖端易損,需謹(jǐn)慎操作;壽命約12–18個(gè)月。
深度假設(shè):默認(rèn)pO????位于切片中點(diǎn)(200μm),實(shí)際可能因組織異質(zhì)性偏移。
替代方案:熒光納米顆粒技術(shù)可空間連續(xù)成像,但成本較高。
核心貢獻(xiàn):Unisense微電極首次將pO????確立為離體腦切片存活度的金標(biāo)準(zhǔn),為神經(jīng)科學(xué)研究提供高效、可靠的質(zhì)控工具。
<strike id="yiuck"></strike>
<strike id="yiuck"></strike>