熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Malaria parasite infection compromises colonization resistance to an enteric pathogen by reducing gastric acidity
瘧疾寄生蟲感染通過降低胃酸度來降低對腸道病原體的定植抵抗力
來源:Walker et al., Sci. Adv. 2021; 7 : eabd6232 30 June 2021
1. 摘要核心內容
本研究揭示瘧原蟲(Plasmodium yoelii)感染通過誘導胃酸減少(低氯hydria),削弱宿主對腸道病原體Salmonella Typhimurium(S. Typhimurium)的定植抵抗力。關鍵發現:
胃酸屏障破壞:瘧原蟲感染小鼠胃pH從2.46升至4.02(圖3B),顯著提升S. Typhimurium在胃中的存活率(圖3A)。
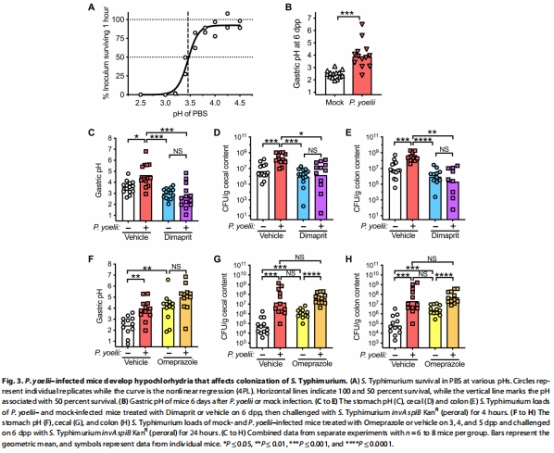
炎癥信號驅動:瘧原蟲感染上調胃組織TNF-α表達(圖4F),阻斷TNF-α信號可恢復胃酸水平及定植抵抗力(圖5B-C)。
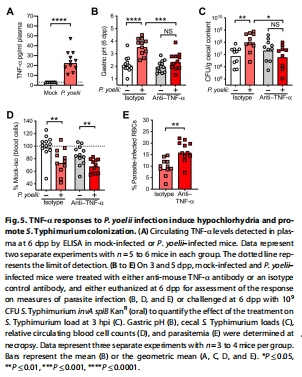
機制驗證:
組胺H2受體激動劑(Dimaprit)刺激胃酸分泌,逆轉瘧疾相關的S. Typhimurium定植增加(圖3C-E);
質子泵抑制劑(Omeprazole)模擬瘧疾效應,升高胃pH并促進病原體定植(圖3F-H)。
2. 研究目的
探究瘧疾患者易并發非傷寒沙門氏菌血癥(NTS)的機制,聚焦瘧原蟲感染如何破壞腸道定植抵抗力,重點關注胃酸屏障的作用。
3. 研究思路
表型觀察→機制排除→核心靶點驗證→臨床關聯:
表型確認:
瘧原蟲感染(6 dpp)顯著提升S. Typhimurium在盲腸和結腸的定植量(10-100倍),且與病原體毒力無關(圖1B-C)。
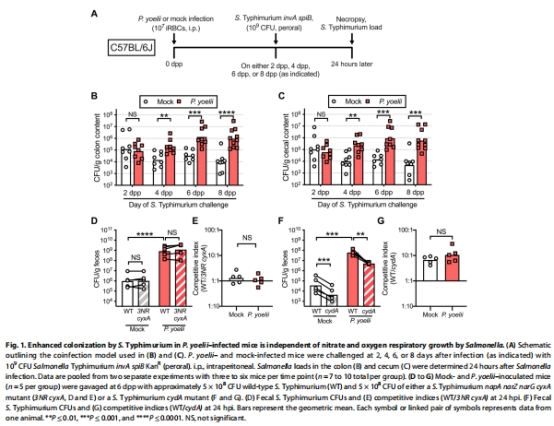
排除次要機制:
硝酸鹽呼吸(napA narZ cyxA突變體)和氧氣呼吸(cydA突變體)非主要因素(圖1D-G);
病原體在腸道內復制速率未增加(圖2A-B)。
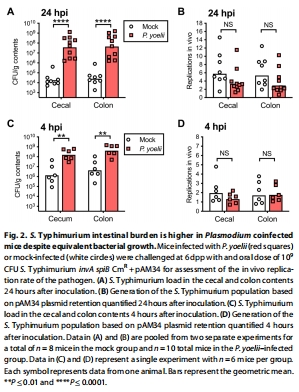
鎖定胃酸屏障:
瘧疾感染導致胃pH升高(圖3B),S. Typhimurium胃存活率與pH負相關(圖3A);
胃酸刺激(Dimaprit)或抑制(Omeprazole)直接調控定植水平(圖3C-H)。
信號通路解析:
TNF-α信號介導胃酸分泌抑制(圖4F,圖5A);
TNF-α抗體阻斷恢復胃酸及定植抵抗力(圖5B-C)。
4. 關鍵數據及研究意義
(1)瘧疾削弱胃酸屏障(圖3)
數據:
胃pH↑63%(2.46→4.02,圖3B);
S. Typhimurium在pH>3.5時存活率↑(圖3A)。
意義:首次證實瘧疾通過低氯hydria突破上消化道防御,為"瘧疾-NTS共感染"提供機制解釋。
(2)炎癥信號TNF-α的核心作用(圖4-5)
數據:
胃組織TnfmRNA↑2.5倍(圖4F),血漿TNF-α↑(圖5A);
TNF-α抗體處理恢復胃pH至正常水平(圖5B),并消除S. Typhimurium定植優勢(圖5C)。
意義:闡明TNF-α→胃酸分泌抑制→病原體存活↑的因果鏈條,提示抗炎策略可輔助防治共感染。
(3)胃酸調控的分子基礎(圖4)
數據:
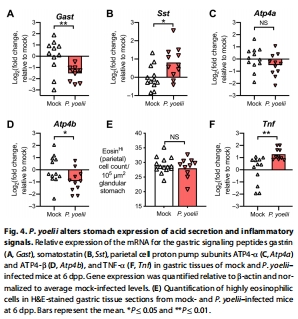
促胃酸激素Gast↓75%,抑胃酸激素Sst↑90%(圖4A-B);
質子泵亞基Atp4bmRNA↓50%(圖4D),但壁細胞數量未變(圖4E)。
意義:揭示瘧疾通過轉錄重編程抑制胃酸分泌,而非細胞損耗。
5. 核心結論
胃酸屏障是定植抵抗力的關鍵:瘧疾誘導的低氯hydria直接提升S. Typhimurium胃存活率,突破腸道定植第一道防線。
TNF-α是核心調控因子:
瘧疾激活TNF-α信號→抑制胃酸分泌基因(Gast↓, Sst↑, Atp4b↓)→胃pH↑;
阻斷TNF-α可逆轉此過程,且不影響瘧原蟲清除(圖5E)。
臨床啟示:
解釋瘧疾流行區NTS感染高發原因;
提示胃酸保護劑(如H2受體激動劑)或抗TNF-α療法可作為輔助治療。
6. 丹麥Unisense電極的研究意義
技術原理與優勢:
微型pH電極(PH-N型):直接插入胃腔實時檢測pH(方法部分);
高精度動態監測:避免離體檢測誤差,實現活體原位測量(圖3B, F)。
關鍵科學貢獻:
定量瘧疾胃酸損傷:
Unisense數據直接顯示:瘧疾感染組胃pH中位數4.02 vs. 對照組2.46(圖3B),為"低氯hydria假說"提供原位實證。
驗證藥物干預效果:
Dimaprit處理使感染組胃pH從4.02降至2.5(圖3C);
Omeprazole處理使對照組胃pH從2.46升至4.0(圖3F),確立胃酸與定植抵抗力的量效關系。
揭示時間動態:
低氯hydria始于感染后6天(dpp),與定植抵抗力喪失同步(圖1A-C),提示胃酸屏障的時效性。
領域突破性價值:
解決傳統終點法(如胃內容物pH試紙)的空間異質性問題,實現活體器官連續pH追蹤;
為胃腸道防御研究提供高時空分辨率工具,推動感染免疫學向動態化發展。
<strike id="yiuck"></strike>
<strike id="yiuck"></strike>