熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Dissolved oxygen from microalgae-gel patch promotes chronic wound healing in diabetes
微藻凝膠貼劑中的溶解氧促進(jìn)糖尿病患者的慢性傷口愈合
來源:Chen et al., Sci. Adv. 2020; 6 : eaba4311 15 May 2020
1. 論文摘要核心內(nèi)容
本研究開發(fā)了一種基于活體微藻水凝膠貼片(AGP)的創(chuàng)新傷口敷料,用于治療糖尿病慢性傷口(如糖尿病足潰瘍):
作用機(jī)制:貼片中的聚球藻(Synechococcus elongatusPCC7942)通過光合作用持續(xù)產(chǎn)生溶解氧(TDO),穿透皮膚效率比傳統(tǒng)氣態(tài)氧療法(TGO)高>100倍(圖1H)。

療效驗(yàn)證:
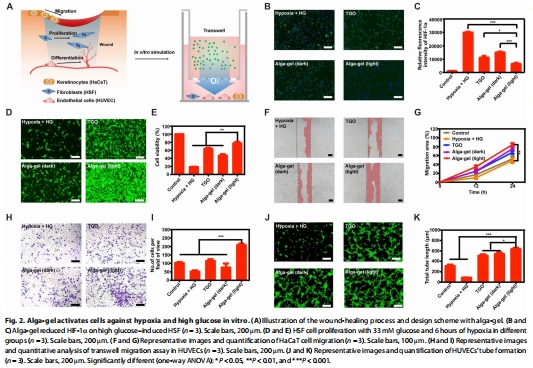
體外促進(jìn)細(xì)胞增殖、遷移和血管形成(圖2);
在糖尿病小鼠模型中加速傷口閉合(45%愈合率 vs. TGO的20%,圖3B),皮瓣存活率提升至82%(對(duì)照組僅3%,圖4C);


將慢性傷口轉(zhuǎn)化為急性愈合表型,下調(diào)缺氧因子HIF-1α,上調(diào)血管生成因子VEGF(圖3J, 4H)。
創(chuàng)新點(diǎn):首款利用生物光合作用持續(xù)供氧的敷料,成本低廉(<1美元/片),兼具抗菌性。
2. 研究目的
1.解決臨床痛點(diǎn):糖尿病慢性傷口因缺氧導(dǎo)致血管生成受損,傳統(tǒng)氧療(如高壓氧HBO、局部氣態(tài)氧TGO)滲透性差、作用短暫。
2.利用溶解氧優(yōu)勢(shì):溶解氧穿透皮膚深度(>700μm)遠(yuǎn)超氣態(tài)氧(300μm),可直達(dá)深層組織(圖1H)。
3.開發(fā)可持續(xù)氧源:通過微藻光合作用實(shí)現(xiàn)持續(xù)、可控的氧釋放。
3. 研究思路
1.貼片設(shè)計(jì)與制備(圖1A-C):
核心結(jié)構(gòu):微藻包裹于海藻酸鈣水凝膠珠(直徑1mm),夾層為親水性聚四氟乙烯(PTFE)膜(允許氣體/水滲透,阻隔細(xì)菌)。
控氧機(jī)制:光照觸發(fā)光合作用產(chǎn)氧,黑暗時(shí)呼吸作用降低氧濃度(圖1D)。
2.體外驗(yàn)證:
氧釋放動(dòng)力學(xué):Unisense電極證實(shí)光照下溶解氧濃度達(dá)600μM(圖1D),碳酸鈉添加進(jìn)一步提升產(chǎn)氧量(圖1F)。
細(xì)胞效應(yīng):AGP促進(jìn)人臍靜脈內(nèi)皮細(xì)胞(HUVEC)、角質(zhì)形成細(xì)胞(HaCaT)遷移和血管形成(圖2F-K)。
3.體內(nèi)療效:
糖尿病小鼠模型:鏈脲佐菌素(STZ)誘導(dǎo)糖尿病,建立全層皮膚缺損傷口。
傷口愈合:AGP治療組12天愈合率達(dá)45%(對(duì)照組20%),上皮化加速(圖3A-D)。
皮瓣存活:AGP組皮瓣壞死率僅18%(TGO組58%),血管密度顯著增加(圖4A-G)。
4. 關(guān)鍵數(shù)據(jù)及研究意義
(1) 溶解氧釋放與皮膚滲透(圖1)
數(shù)據(jù):
光照下溶解氧濃度30分鐘內(nèi)從0升至600μM(圖1D);
穿透小鼠皮膚后,AGP組氧濃度達(dá)240μM,TGO組幾乎為0(圖1H)。
意義:直接證明溶解氧穿透皮膚的高效性,為AGP的臨床優(yōu)勢(shì)提供核心證據(jù)。
(2) 體外細(xì)胞功能促進(jìn)(圖2)
數(shù)據(jù):
AGP使HUVEC遷移率提升2倍(圖2H-I),血管形成能力增強(qiáng)(管長度+40%,圖2J-K);
下調(diào)缺氧標(biāo)志物HIF-1α(圖2B-C)。
意義:揭示AGP通過改善缺氧微環(huán)境促進(jìn)細(xì)胞修復(fù)功能。
(3) 動(dòng)物模型療效(圖3-4)
數(shù)據(jù):
傷口愈合:AGP組第6天愈合率45%(TGO組20%),膠原沉積增加(圖3D,H);
皮瓣存活:AGP組血管密度達(dá)66.9%(對(duì)照組13.1%),HIF-1α表達(dá)降低(圖4E-G);
分子機(jī)制:VEGF/HIF-1α比值提升2.48倍(圖4I)。
意義:證實(shí)AGP通過促血管生成和緩解缺氧加速傷口愈合。
(4) 安全性及穩(wěn)定性(圖1I)
數(shù)據(jù):AGP在4°C儲(chǔ)存15天仍保持>1000μM氧釋放能力(圖1I)。
意義:確保臨床應(yīng)用的可行性與長效性。
5. 丹麥Unisense電極的核心價(jià)值
(1) 技術(shù)原理
功能:實(shí)時(shí)監(jiān)測(cè)溶液中溶解氧(DO)濃度動(dòng)態(tài)變化(方法2.6)。
實(shí)驗(yàn)設(shè)計(jì):用于量化AGP在不同條件下的氧釋放動(dòng)力學(xué)(圖1D-F)。
(2) 關(guān)鍵發(fā)現(xiàn)(圖1D-F)
光控氧釋放:光照30分鐘DO從0→600μM,黑暗時(shí)反向下降(圖1D),證明微藻光合/呼吸作用的可控性。
碳酸鈉增強(qiáng)效應(yīng):添加500μM Na?CO?使DO峰值提升至1400μM(圖1F),為配方優(yōu)化提供依據(jù)。
緩釋特性:DO濃度隨時(shí)間呈緩釋曲線(30分鐘達(dá)平臺(tái)期),符合治療需求。
(3) 研究意義
機(jī)制驗(yàn)證:直接量化AGP的氧釋放能力,排除間接檢測(cè)方法(如熒光探針)的誤差風(fēng)險(xiǎn)。
劑量優(yōu)化:確定微藻最佳濃度(1×10? cells/ml,圖1E)和碳酸鈉添加量,最大化療效。
技術(shù)優(yōu)勢(shì):高時(shí)空分辨率捕捉動(dòng)態(tài)過程(秒級(jí)響應(yīng)),優(yōu)于傳統(tǒng)終點(diǎn)法檢測(cè)。
6. 結(jié)論
1.AGP有效性:溶解氧穿透深度>100倍于氣態(tài)氧,顯著加速糖尿病傷口愈合(12天愈合率45%)和皮瓣存活(壞死率降至18%)。
2.機(jī)制明確:通過下調(diào)HIF-1α、上調(diào)VEGF,促進(jìn)血管生成,逆轉(zhuǎn)慢性傷口缺氧微環(huán)境。
3.臨床價(jià)值:低成本(<1美元/片)、長效穩(wěn)定(15天活性)、無免疫原性,為糖尿病足潰瘍提供革新療法。
4.Unisense電極貢獻(xiàn):精準(zhǔn)量化氧釋放動(dòng)力學(xué),為AGP的設(shè)計(jì)優(yōu)化和機(jī)制闡釋提供不可替代的數(shù)據(jù)支持。
總結(jié)
本研究通過丹麥Unisense電極的動(dòng)態(tài)監(jiān)測(cè),結(jié)合多維度實(shí)驗(yàn)驗(yàn)證,首次闡明:
1.溶解氧的核心優(yōu)勢(shì):高效穿透皮膚,直達(dá)深層缺氧組織;
2.AGP的設(shè)計(jì)科學(xué)性:微藻光合作用提供持續(xù)、可控氧源;
3.Unisense技術(shù)的不可替代性:
實(shí)時(shí)捕捉氧釋放動(dòng)力學(xué),指導(dǎo)劑量優(yōu)化;
驗(yàn)證光照/黑暗切換的氧控能力;
為轉(zhuǎn)化醫(yī)學(xué)提供精準(zhǔn)數(shù)據(jù)支撐。
該研究為糖尿病慢性傷口治療開辟了新途徑,Unisense電極在此過程中發(fā)揮了關(guān)鍵的機(jī)制解碼和技術(shù)優(yōu)化作用。
<strike id="yiuck"></strike>
<strike id="yiuck"></strike>