熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
pH-Responsive Oxygen Nanobubbles for Spontaneous Oxygen Delivery in Hypoxic Tumors
pH響應性氧納米氣泡用于缺氧腫瘤中自發性氧輸送
來源:Langmuir, volume 35,2019,pages 10166-10172
《朗繆爾》,第35卷,2019年,頁碼10166-10172
摘要
這篇論文研究了一種pH響應性氧納米氣泡,用于解決腫瘤缺氧導致的治療抵抗問題。摘要指出,腫瘤缺氧是光動力療法和放療等氧依賴療法失敗的主要原因。傳統氧輸送系統如全氟碳納米乳劑和脂質氧微泡存在氧提前釋放和依賴外部刺激的缺點。本研究開發了由乙酰化葡聚糖(AC-DEX)聚合物殼包裹的氧納米氣泡,能在腫瘤微環境pH下降時自發性釋放氧。納米氣泡在循環血液中穩定,保留氧負載,在酸性環境中爆發釋放。體外和體內實驗表明,納米氣泡具有良好穩定性和生物相容性。在CNE2腫瘤小鼠模型中,納米氣泡使腫瘤內氧水平提高了6倍,顯示其作為氧輸送劑的潛力,以克服缺氧誘導的抵抗。
研究目的
研究目的是開發一種無需外部刺激的pH響應性氧納米氣泡,用于高效、自發性氧輸送至缺氧腫瘤,以增強氧依賴療法的效果,并解決傳統氧輸送系統的局限性,如提前釋放和外部依賴。
研究思路
研究思路是合成乙酰化葡聚糖(AC-DEX)作為pH響應性聚合物殼,通過乳液-溶劑蒸發法制備氧納米氣泡。納米氣泡由AC-DEX殼和脂質外層組成,以增強穩定性和生物相容性。評估納米氣泡的物理特性(尺寸、結構)、超聲性能、細胞毒性、體外pH響應性氧釋放,以及在體內使用CNE2腫瘤小鼠模型測量腫瘤氧水平變化。使用丹麥Unisense微電極實時監測腫瘤內氧分壓,驗證氧輸送效率。
測量的數據及研究意義
1 納米氣泡尺寸和zeta電位數據來自圖3a,尺寸為325.4±12.5 nm,zeta電位為-13.2±2.1 mV。研究意義是確認納米氣泡大小適合通過腫瘤血管內皮間隙(400-800 nm),實現被動靶向和EPR效應,確保腫瘤積累。

2 納米氣泡結構數據來自圖3b,顯示核心-殼結構和光滑表面。研究意義是驗證納米氣泡的成功制備和形態,支持其作為氣體載體的功能。
3 超聲成像數據來自圖4,顯示納米氣泡濃度依賴的超聲對比增強。研究意義是證明納米氣泡可作為超聲對比劑,用于成像引導的氧輸送和實時監測。

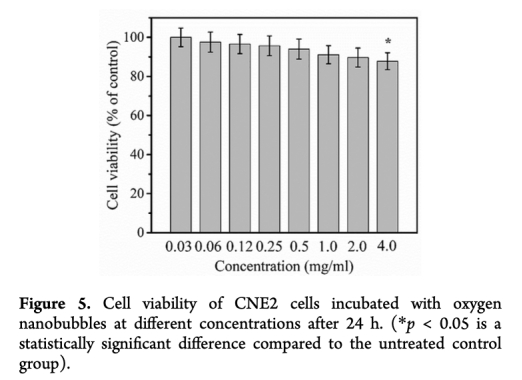
4 細胞毒性數據來自圖5,顯示CNE2細胞在納米氣泡處理24小時后活力無顯著變化。研究意義是表明納米氣泡具有良好生物相容性,無細胞毒性,適合體內應用。
5 體外氧釋放動力學數據來自圖6a,顯示在pH 6.5和7.4條件下氧釋放曲線,pH 6.5時釋放更快。研究意義是證實納米氣泡的pH響應性,在酸性環境中加速氧釋放,模擬腫瘤微環境。

6 體內氧分壓數據來自圖7b,使用丹麥Unisense微電極測量,顯示腫瘤內pO2在納米氣泡注射后增加約6倍。研究意義是直接證明納米氣泡在體內有效提高腫瘤氧水平,緩解缺氧,增強治療效果。

7 組織學數據,顯示主要器官(心、肝、脾、肺、腎)H&E染色無異常。研究意義是評估納米氣泡的全身生物安全性,確認無器官損傷。
結論
論文得出結論,pH響應性氧納米氣泡能穩定輸送氧,在腫瘤酸性環境中自發性爆發釋放,顯著提高腫瘤氧水平(6倍增加)。納米氣泡具有良好穩定性和生物相容性,無需外部刺激,能有效克服腫瘤缺氧,改善氧依賴療法的療效,如放療和光動力療法。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense微電極測量的數據是腫瘤內氧分壓(pO2)的變化(圖7b),研究意義在于提供實時、準確的體內氧水平量化,直接驗證納米氣泡的氧輸送效率。測量顯示pO2從基線約4 mmHg增加到峰值約24 mmHg,并維持高水平超過2小時,這證實納米氣泡能有效緩解腫瘤缺氧,為放療和光動力療法提供足夠的氧支持(pO2 >20 mmHg可減少輻射抵抗)。這種精確測量確保了實驗的可靠性,并突出了納米氣泡在臨床轉化中的潛力,無需侵入性操作或外部激活。
<strike id="yiuck"></strike>
<strike id="yiuck"></strike>