熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Online oxygen monitoring using integrated inkjet-printed sensors in a liver-on-a-chip system
在芯片上的肝臟系統(tǒng)中使用集成的噴墨打印傳感器進(jìn)行在線氧監(jiān)測
來源:Lab Chip, 2018, 18, 2023
論文總結(jié)
研究通過噴墨打印技術(shù)(IJP)在肝臟芯片(liver-on-a-chip)系統(tǒng)中集成溶解氧(DO)傳感器,實現(xiàn)實時監(jiān)測氧氣濃度梯度,以揭示肝細(xì)胞代謝分區(qū)(zonation)機制。以下從摘要、研究目的、研究思路、測量數(shù)據(jù)及意義、結(jié)論等方面進(jìn)行總結(jié),并詳細(xì)解讀使用丹麥Unisense電極測量數(shù)據(jù)的意義。
一、論文摘要
研究開發(fā)了一種在肝臟芯片系統(tǒng)(ExoLiver)中集成噴墨打印DO傳感器的方法,用于實時監(jiān)測微環(huán)境中的氧氣濃度。傳感器被打印在超薄多孔膜(65μm厚,80%孔隙率)上,通過SU-8 primer層密封孔隙,形成金和銀電極。三個傳感器沿微流體通道放置(流入、中間、流出點),允許局部監(jiān)測氧氣梯度。實驗顯示,大鼠和人類肝細(xì)胞存在顯著氧氣梯度(大鼠高達(dá)17.5%,人類高達(dá)32.5%),且使用線粒體解耦劑FCCP刺激后,氧消耗率(OCR)顯著增加(大鼠從0.23增至5.95 nmol s?1/10? cells,人類從0.17增至10.62 nmol s?1/10? cells)。結(jié)果表明,IJP技術(shù)能成功集成傳感器于脆弱基板,實現(xiàn)實時監(jiān)測,克服了器官芯片(OOC)系統(tǒng)監(jiān)測的挑戰(zhàn)。
二、研究目的
實現(xiàn)實時監(jiān)測:解決OOC系統(tǒng)中細(xì)胞功能監(jiān)測的難題,特別是氧氣濃度變化,以更好地理解肝細(xì)胞代謝和分區(qū)。
集成傳感器:通過IJP技術(shù)在多孔膜上直接打印傳感器,避免傳統(tǒng)方法的高溫、復(fù)雜工藝和不兼容性問題。
驗證生物學(xué)應(yīng)用:使用原代大鼠和人類肝細(xì)胞,驗證傳感器在監(jiān)測氧氣梯度、OCR和藥物響應(yīng)(如FCCP)中的有效性。
促進(jìn)器官芯片發(fā)展:為OOC系統(tǒng)提供低成本、高靈活性的傳感集成方案,提升其預(yù)測性和臨床應(yīng)用潛力。
背景基于OOC系統(tǒng)在模擬器官生理中的重要性,但傳統(tǒng)監(jiān)測方法(如光學(xué)顯微鏡或外部探頭)無法實現(xiàn)實時、多點、非侵入式測量,尤其在高密度細(xì)胞培養(yǎng)中。
三、研究思路
研究采用噴墨打印技術(shù)與微流體系統(tǒng)結(jié)合的策略:
傳感器制造:使用IJP在多孔PTFE膜上打印SU-8 primer層(密封孔隙),然后打印金(工作電極和計數(shù)電極)和銀(偽參考電極)墨水,形成電化學(xué)DO傳感器(Fig. 1)。打印后熱燒結(jié)(130°C,40分鐘)和UV固化,確保電極導(dǎo)電性和穩(wěn)定性。
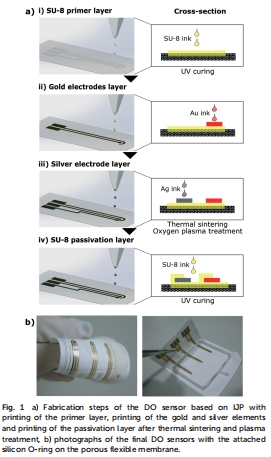
系統(tǒng)集成:將三個傳感器集成于ExoLiver生物反應(yīng)器的多孔膜上,沿微流體通道分布(流入、中間、流出點),與細(xì)胞培養(yǎng)區(qū)域直接接觸(Fig. 3)。系統(tǒng)包括上通道(流動培養(yǎng)基)和下通道(靜態(tài)肝細(xì)胞培養(yǎng))。
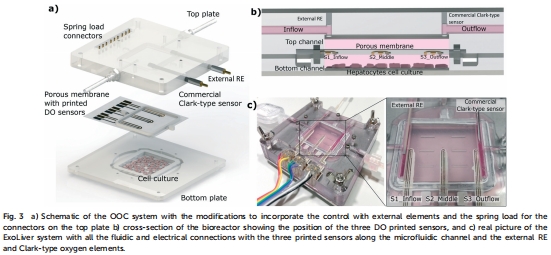
實驗驗證:使用原代大鼠和人類肝細(xì)胞培養(yǎng),通過微流體灌注維持細(xì)胞活力。添加FCCP(0.5μM步驟)刺激OCR,監(jiān)測氧氣變化。使用商業(yè)Unisense Clark型電極作為參考驗證。
數(shù)據(jù)分析:通過安培法(-650 mV極化)測量DO,校準(zhǔn)傳感器(線性范圍0-9 mg L?1)。建立數(shù)學(xué)模型估計OCR(基于質(zhì)量平衡和Michaelis-Menten動力學(xué)),并比較細(xì)胞響應(yīng)。
四、測量數(shù)據(jù)、來源及研究意義
研究測量了多維度數(shù)據(jù),其意義及來源如下(數(shù)據(jù)均標(biāo)注自原文圖/表):
傳感器性能數(shù)據(jù)(數(shù)據(jù)來自校準(zhǔn)曲線):
數(shù)據(jù):傳感器線性范圍0-9 mg L?1,靈敏度28±1 nA L mg?1,檢測限0.11±0.02 mg L?1,Sheet電阻<2 Ω□?1。
研究意義:證實IJP傳感器具有高靈敏度和可靠性,適用于生物環(huán)境;低檢測限允許精確監(jiān)測低氧條件,為實時監(jiān)測提供基礎(chǔ)。
氧氣梯度監(jiān)測(數(shù)據(jù)來自Fig. 4):

數(shù)據(jù):在肝細(xì)胞培養(yǎng)中,流入點DO最高,流出點最低。大鼠肝細(xì)胞梯度達(dá)17.5%(如從~6.5 mg L?1降至~5.4 mg L?1),人類肝細(xì)胞梯度達(dá)32.5%(如從~6.0 mg L?1降至~4.0 mg L?1)。無細(xì)胞對照無梯度(Fig. 4a)。
研究意義:直接驗證肝竇狀隙中氧氣梯度的存在,模擬體內(nèi)分區(qū)(zonation)現(xiàn)象;梯度大小反映物種差異,人類肝細(xì)胞對氧更敏感,支持個性化醫(yī)學(xué)模型。
氧消耗率(OCR)估計(數(shù)據(jù)來自Fig. 5和數(shù)學(xué)模型):
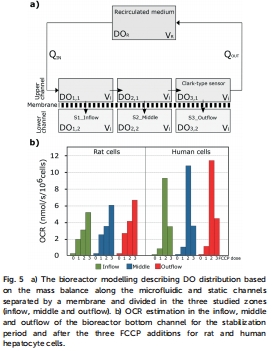
數(shù)據(jù):基礎(chǔ)OCR大鼠為0.23±0.07 nmol s?1/10? cells,人類為0.17±0.10 nmol s?1/10? cells。FCCP刺激后,OCR大幅增加(大鼠至5.95±0.67 nmol s?1/10? cells,人類至10.62±1.15 nmol s?1/10? cells)。流出點OCR比流入點高1.2倍(大鼠)和1.4倍(人類)。
研究意義:量化細(xì)胞代謝響應(yīng),揭示FCCP通過解耦線粒體增加呼吸;OCR梯度證實細(xì)胞適應(yīng)低氧環(huán)境,轉(zhuǎn)向糖酵解,與腫瘤代謝類似,為藥物測試提供模型。
細(xì)胞存活與形態(tài)(數(shù)據(jù)來自Fig. 4d):
數(shù)據(jù):顯微鏡圖像顯示肝細(xì)胞在實驗開始和結(jié)束時保持多邊形形態(tài)和高存活率,無顯著死亡或形態(tài)變化。
研究意義:證實傳感器集成和低氧條件不影響細(xì)胞健康,支持方法的生物相容性;細(xì)胞在低氧下維持功能,可能通過 anaerobic glycolysis 適應(yīng)。
與商業(yè)傳感器比較(數(shù)據(jù)來自Fig. 4黑線):
數(shù)據(jù):Unisense Clark型傳感器(上通道流出點)測量與打印傳感器一致,但僅能提供單點數(shù)據(jù),無法捕獲梯度。
研究意義:驗證打印傳感器的準(zhǔn)確性;突出集成傳感器的優(yōu)勢——多點監(jiān)測能力,克服商業(yè)傳感器的空間限制。
五、研究結(jié)論
成功集成傳感器:IJP技術(shù)能在多孔膜上可靠打印DO傳感器,無需高溫或復(fù)雜工藝,實現(xiàn)OOC系統(tǒng)內(nèi)置監(jiān)測。
氧氣梯度證實:肝細(xì)胞培養(yǎng)中存在顯著氧氣梯度(高達(dá)32.5%),模擬體內(nèi)分區(qū),對人類肝細(xì)胞更明顯。
代謝響應(yīng)量化:FCCP刺激顯著增加OCR,揭示細(xì)胞代謝靈活性;流出點細(xì)胞OCR更高,表明適應(yīng)低氧。
技術(shù)優(yōu)勢:打印傳感器提供實時、多點、非侵入式監(jiān)測,優(yōu)于傳統(tǒng)方法;模型支持OCR估計,增強數(shù)據(jù)解讀。
應(yīng)用前景:方法可擴展至其他參數(shù)(如pH、葡萄糖)監(jiān)測,推動OOC系統(tǒng)在藥物篩選和疾病建模中的應(yīng)用。
六、詳細(xì)解讀使用丹麥Unisense電極測量出來的數(shù)據(jù)有什么研究意義
丹麥Unisense電極(具體為Clark型氧微電極,型號OX-NP)在本研究中作為參考傳感器,用于驗證打印傳感器的準(zhǔn)確性和可靠性。其研究意義如下:
提供金標(biāo)準(zhǔn)驗證:
技術(shù)描述:Unisense電極基于Clark原理,具有高精度(檢測限低)和快速響應(yīng)(每秒測量),常用于生物醫(yī)學(xué)研究。在本研究中,它被放置于生物反應(yīng)器的上通道流出點,提供連續(xù)DO測量(Fig. 3c)。
研究應(yīng)用:與打印傳感器數(shù)據(jù)比較(Fig. 4),顯示高度一致性(如DO濃度趨勢匹配),確認(rèn)打印傳感器的校準(zhǔn)和性能(線性響應(yīng)和靈敏度)。
研究意義:作為獨立驗證工具,Unisense電極確保了打印傳感器的數(shù)據(jù)可靠性,減少了系統(tǒng)誤差,為新技術(shù) adoption 提供可信度。
突出集成傳感器的優(yōu)勢:
局限性分析:Unisense電極雖精確,但僅能提供單點測量(上通道),無法直接監(jiān)測細(xì)胞附近的梯度(下通道)。這是由于它的尺寸和位置限制——需插入系統(tǒng),可能干擾微環(huán)境。
研究意義:通過對比,凸顯打印傳感器的獨特價值:能嵌入細(xì)胞培養(yǎng)膜(下通道),實現(xiàn)多點、原位監(jiān)測(流入、中間、流出點),直接捕獲氧氣梯度(如Fig. 4b-c所示梯度),而Unisense只能間接推斷。這強調(diào)了集成傳感對于OOC系統(tǒng)全面監(jiān)測的必要性。
支持生物學(xué)發(fā)現(xiàn):
數(shù)據(jù)關(guān)聯(lián):Unisense數(shù)據(jù)幫助確認(rèn)FCCP添加后的氧消耗變化(如Fig. 4中黑線下降),與打印傳感器響應(yīng)同步,證實藥物效應(yīng)。
研究意義:驗證了細(xì)胞代謝響應(yīng)的真實性,如OCR增加;Unisense的連續(xù)監(jiān)測(每秒)補充了打印傳感器的間歇測量(每15分鐘),提供更動態(tài)的視圖,但打印傳感器提供了空間分辨率。
技術(shù)互補性與未來方向:
協(xié)同作用:Unisense電極用于校準(zhǔn)和關(guān)鍵時刻驗證,而打印傳感器用于日常監(jiān)測,降低成本和復(fù)雜性。
研究意義:展示了多傳感器融合的策略——Unisense作為“黃金標(biāo)準(zhǔn)”用于方法開發(fā),打印傳感器用于規(guī)模化應(yīng)用。這為OOC系統(tǒng)的標(biāo)準(zhǔn)化監(jiān)測提供了藍(lán)圖,鼓勵開發(fā)更多集成傳感器(如用于pH或代謝物)。
總之,Unisense電極在本研究中是質(zhì)量控制的關(guān)鍵工具,其數(shù)據(jù)不僅驗證了打印傳感器的性能,還強調(diào)了在復(fù)雜生物系統(tǒng)中多點監(jiān)測的重要性。這推動了OOC監(jiān)測從單一外部測量向內(nèi)部、實時、多維發(fā)展的演進(jìn),有望加速器官芯片在精準(zhǔn)醫(yī)學(xué)和藥物開發(fā)中的轉(zhuǎn)化。
<strike id="yiuck"></strike>
<strike id="yiuck"></strike>